INFERTILITÀ DI COPPIA
Si parla di infertilità quando una coppia, per cause femminili o maschili, non riesce ad ottenere una gravidanza dopo un anno di rapporti costanti e non protetti.
E’ quindi una condizione potenzialmente reversibile.
Il termine sterilità, invece, si riferisce ad una condizione assoluta e potenzialmente risolvibile solo con procedimenti medici invasivi.
INFERTILITÀ E RIPRODUZIONE MEDICALMENTE ASSISTITA
Introduzione
Alla nascita, ogni donna possiede circa 1-2 milioni di ovociti. Al momento dello sviluppo (pubertà), questo numero è già ridotto a 300-500 mila e questo patrimonio di uova (riserva ovarica) andrà via via impoverendosi sino alla menopausa. Le cellule uovo sono immagazzinate nelle due ovaie all’interno di piccole strutture dette follicoli ovarici primordiali. A ogni ciclo mestruale in genere un ovocita solo giunge a maturazione (ovulazione) e contemporaneamente molti altri (50-100), che erano stati preparati per partecipare alla competizione che ha scelto il vincitore, “vanno in atresia” (ossia scompaiono), sino a che l’intera riserva ovarica si annulla o quasi. A questo punto la donna entra in menopausa (assenza di mestruazione da almeno sei mesi), sebbene sia uscita dall’età fertile circa sette anni prima di questo fenomeno. Negli anni che precedono la menopausa, infatti, la donna, pur avendo un ciclo mestruale regolare o abbastanza regolare, ha una ridottissima possibilità di concepire a causa di un ridotto numero e qualità di ovociti residui. Il fenomeno del consumo mensile degli ovociti è il vero fenomeno limitante della fertilità femminile e appare un elemento inarrestabile. Non si ferma infatti nel periodo della gravidanza, o per l’assunzione di estroprogestinici (pillola contraccettiva) o altri farmaci. Il numero iniziale di ovociti è determinato nel corso della vita intrauterina (attorno alla ventesima settimana di gravidanza) ed è diverso alla nascita da donna a donna. Condizioni genetiche, familiari o altri fattori come alcune sostanze tossiche ambientali o farmacologiche possono ridurre, modificare o accelerare il consumo di questa riserva di ovociti e giustificano quindi un’epoca diversa per ogni donna sull’insorgere della menopausa.
Durante la fase fertile della vita di una donna, il rilascio dell’ovocita maturo (ovulazione) avviene all’incirca ogni quattro settimane. Avvenuta l’ovulazione, l’ovocita viene catturato da strutture simili a dita localizzate sulla parte terminale delle tube di Faloppio, denominate “fimbrie”.
La salpinge o tuba di Fallopio una struttura dotata di uno spazio virtuale e collega la cavità uterina con la cavità addominale. E’ responsabile del trasporto attivo degli spermatozoi che dalla cervice, attraverso la cavità uterina devono raggiungere la parte terminale della salpinge (ampolla) e/o giungere nello scavo del Douglas. Questo spazio posteriore all’utero in cui le ovaie e gli ovociti galleggiano nei fluidi prodotti dagli organi della pelvi e dal liquido contenuto nel follicolo maturo e viene anche definito con un termine antico ma efficace, pozzo della fertilità. Lo spermatozoo grazie alla sua motilità e a modificazioni della quantità e delle caratteristiche del muco cervicale, viene protetto dalla vagina che lo ucciderebbe in pochi minuti. Una volta entrato nel collo dell’utero viene protetto dalle cripte cervicali e dopo modificazioni della sua struttura (capacitazione) acquisisce una motilità attiva che gli consente di attraversare la cavità uterina (endometrio) e raggiugere le tube. E’ favorito in questo processo dalla contrazione degli stati muscolari dell’utero che hanno comportamenti diversi in relazione alla fase del ciclo e ai livelli ormonali raggiunti nel periodo ovulatorio. Questo trasporto attivo può prescindere dal movimento degli spermatozoi, infatti particelle delle dimensioni dello spermatozoo poste in vagina possono raggiungere in questo periodo l’addome della donna in pochi minuti.
E’ proprio all’interno delle fimbrie tubariche che gli ovociti possono essere fecondati dagli spermatozoi, sebbene l’ovocita fecondato possa catturato dalle fimbrie all’interno della pelvi attraverso sottili meccanismi di riconoscimento e attrazione. Dopo la fecondazione, l’ovocita fecondato (zigote) percorre la salpinge, grazie a ciglia vibratili che ne permettono il movimento e lo sospingono verso l’utero, associate a movimenti peristaltici della muscolatura della tuba stessa che favoriscono la progressione dell’embrione. Nel corso di questo percorso l’ovocita fecondato si sviluppa in modo progressivo dalle due cellule (blastomeri) che compongono l’embrione nelle fasi iniziali della divisione cellulare (embrione allo stadio di clivaggio), sino alle oltre 100 – 150 cellule raggiunte dopo cinque – sei giorni di sviluppo e dalla divisione nelle cellule che daranno origine all’embrione e da quelle che daranno origine alla placenta (embrione allo stadio di blastocisti). E’ a questo grado di sviluppo che l’embrione entra nella cavità uterina, dove il rivestimento interno dell’utero (endometrio) si ispessisce e acquisisce le caratteristiche adatte all’impianto dell’embrione.
Se l’ovocita non viene fecondato, oppure l’embrione ha subito un arresto nel suo sviluppo o non riesce ad impiantarsi nella cavità uterina, l’endometrio si sfalda, staccandosi dalle pareti uterine e provocando quindi la mestruazione.
Il ciclo mestruale
Nella maggior parte delle donne, un ciclo mestruale dura 28 giorni, ma ci possono essere variazioni da donna a donna e, talvolta, da ciclo a ciclo anche nella stessa persona.
La prima parte del ciclo prende il nome di fase follicolare e inizia quando nel sangue si abbassano i livelli di ormoni femminili (estrogeni e progesterone). Il giorno di arrivo della mestruazione è convenzionalmente indicato come 1° giorno del ciclo. Questa diminuzione degli estrogeni che avviene nella fase mestruale e premestruale fa sì che l’ipotalamo, una ghiandola localizzata alla base del cervello, rilasci una molecola ormonale chiamata GnRH che, a sua volta, stimola l’ipofisi (una seconda piccola ghiandola localizzata nel cervello) a produrre altri due ormoni (gonadotropine), detti FSH (ormone follicolo stimolante) ed LH (ormone luteinizzante), responsabili dello sviluppo e maturazione degli ovociti.
L’FSH stimola lo sviluppo di molti follicoli ovarici che dopo un lungo percorso durato mesi, giungono a essere sensibili a questa sostanza (follicoli antrali). Le cellule dei follicoli antrali (cellule della granulosa) producono gli estrogeni necessari affinché l’endometrio cresca per accogliere l‘embrione nella cavità dell’utero, raggiunto il corretto grado di sviluppo e nel giusto momento di maturazione endometriale (finestra di impianto). Grazie ad un sistema di feedback, l’aumento degli estrogeni è un segnale per il cervello, che riduce la produzione di GnRH e, di conseguenza, quella di FSH. A questo punto lo sviluppo dei follicoli si arresta e tutti si fermano, tranne uno, in genere, il follicolo dominante.
Questi meccanismi che regolano l’attività dell’ipotalamo, ipofisi e ovaio (follicologenesi) sono straordinariamente complessi e regolati da numerose altre molecole e condizioni e sono tuttora oggetto di studi e ricerche per il loro meraviglioso interesse non solo in campo riproduttivo.
Quando i livelli di estrogeni sono sufficientemente elevati per un numero minimo di giorni, questo fenomeno induce l’ipofisi a un aumento improvviso dei livelli di LH ( picco di LH) che induce la maturazione finale dell’ovocita e il suo rilascio. Nelle 24-36 ore successive ha luogo l’ovulazione, che non è altro che la rottura del follicolo e il rilascio del liquido in esso contenuto e dell’ovocita nella cavità addominale. Dato che il picco di LH si realizza intorno al 12° giorno di un ciclo mestruale tipico, il giorno dell’ovulazione è all’incirca il 14°.
Con l’ovulazione ha inizio la 2° parte del ciclo mestruale (fase luteale), che prosegue fino alla comparsa della mestruazione. In questa fase, mentre l’ovocita o l’embrione percorrono una delle due tube di Falloppio per raggiungere l’utero, ma anche in assenza di questo fenomeno, il follicolo ovarico, rimasto vuoto, si trasforma in corpo luteo (formazione cistica chiamata così per il colore giallastro) che, oltre a continuare la produzione di estrogeni, è responsabile dell’aumento del progesterone. Questi due ormoni (estrogeni e progesterone) conducono alle modifiche dell’endometrio per renderlo adatto a un eventuale impianto di gravidanza e, contemporaneamente (attraverso un meccanismo di feedback) sopprimono la sintesi di gonadotropine da parte dell’ipofisi.
Se l’ovocita non viene fecondato, dopo circa 10 giorni il corpo luteo inizia a regredire. Di conseguenza, i livelli di estrogeni e di progesterone diminuiscono drasticamente, portando al progressivo sfaldamento dell’endometrio, con comparsa della mestruazione. In una donna con cicli regolari, ogni mestruazione avviene 28 giorni dopo la precedente. Con l’arrivo del flusso mestruale, ricomincia la produzione di GnRH da parte dell’ipotalamo e un altro ciclo ha inizio.
Il sistema riproduttivo maschile
Come abbiamo visto, la donna, dopo la nascita, non può più aumentare la sua riserva ovarica; per l’uomo, invece, le cose vanno in modo diverso. La produzione degli spermatozoi inizia, infatti, con la pubertà e continua per tutto il resto della vita. A controllarla sono gli stessi ormoni che regolano il ciclo mestruale femminile: GnRH, LH e FSH.
La successiva maturazione delle cellule spermatiche è resa possibile dal testosterone, l’ormone prodotto dagli organi sessuali maschili, responsabile del passaggio verso la pubertà e l’età fertile matura nel sesso maschile. I suoi livelli sono attentamente controllati dal cervello: quando sono sufficienti, la produzione di GnRH e, di conseguenza, di LH e FSH diminuisce, ma se i testicoli producono poco testosterone, il cervello riceve un segnale per aumentare la produzione di GnRH e, quindi, di gonadotropine.
La sintesi del testosterone inizia durante la pubertà e raggiunge un picco tra i 25 e i 30 anni, dopo i quali inizia a diminuire.
Il viaggio degli spermatozoi
Gli spermatozoi sono prodotti da sottili strutture tubulari presenti all’interno dei testicoli (a loro volta contenuti nello scroto) attraverso una serie di divisioni e differenziazioni cellulari che richiedono 2-3 mesi per essere portate a termine. Dato che questo processo inizia in momenti diversi all’interno di migliaia di tubuli, ogni uomo ha sempre a disposizione una riserva di spermatozoi maturi.
Gli spermatozoi sono convogliati all’esterno dei testicoli attraverso una rete di tubuli che giunge all’epididimo, (un groviglio di sottili tubi che raggiungono la lunghezza complessiva di 6-7 metri) che collega il testicolo col dotto deferente. L’epididimo ospita gli spermatozoi per almeno una settimana, periodo durante il quale il loro processo di maturazione continua ed essi acquistano una maggiore capacità di movimento. Al momento dell’eiaculazione gli spermatozoi, passando attraverso il dotto deferente, si uniscono al prodotto di ghiandole accessorie (prostata, vescicole seminali) formando lo sperma.
Il destino finale dello sperma è di essere espulso durante l’eiaculazione attraverso l’uretra, canale che percorre il pene. Un uomo “normospermico” eiacula tra 1,5 e 6 millilitri di sperma, contenente da 20 a 200 milioni di spermatozoi per ogni millilitro.
La fecondazione
Dopo circa mezz’ora dalla sua deposizione, lo sperma denso e viscoso eiaculato in vagina subisce una trasformazione che lo rende più fluido. La maggior parte degli spermatozoi fisiologicamente non riesce a risalire il canale cervicale, l’organo che collega la vagina alla cavità uterina. Infatti, solo durante il periodo periovulatorio della donna, il muco cervicale favorisce la sopravvivenza degli spermatozoi e importanti modificazioni degli stessi, rendendoli capaci di superare l’ambiente cervicale e di iniziare la corsa che li porterà a poter fertilizzare la cellula uovo.
A questo punto, solo alcune migliaia di spermatozoi giunti in cavità uterina sono in grado di proseguire il loro percorso attraverso le tube di Falloppio, e circa 200 arrivano a poter incontrare l’ovocita pronto per essere fecondato.
Dopo l’ovulazione e durante la sua permanenza nella tuba l’ovocita ha circa 24 ore di tempo per essere fecondato. Lo spermatozoo, invece, può mantenere le sue capacità fecondanti fino a 3-4 giorni dopo l’eiaculazione, sebbene siano provati concepimenti sino a 17 giorni antecedenti il momento dell’ovulazione. Ciò significa che, in realtà ogni rapporto in ogni fase del ciclo ha una probabilità di essere fecondo, sebbene sia maggiore se il rapporto precede l’ovulazione.
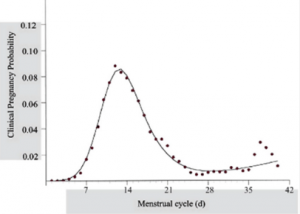
Probabilità di gravidanza (fecondabilità) per singolo rapporto. Per questo ogni metodo di ricerca del periodo ovulatorio viene giudicato inaccurato e persino dannoso in termini di probabilità di concepire. Le coppie fertili che voglio concepire hanno una maggiore probabilità di concepimento (37% per ciclo) se hanno rapporti quotidiani. Rapporti a giorni alterni conducono ad una fecondabilità comparabile (33%), ma le probabilità di concepire si riducono al15% per rapporti una volta a settimana. Lo stress associato al desiderio di concepire possono ridurre il piacere nell’avere rapporti, la propria autostima sessuale e la frequenza dei rapporti stessi. Un rapporto piacevole conduce da solo ad una maggiore probabilità di essere fecondante.
In questo lasso di tempo lo spermatozoo deve raggiungere la parte terminale della tuba ed entrare nell’ovocita (fecondazione), promuovendone la definitiva maturazione. La cellula risultante da questa fusione (zigote) inizia il suo transito verso l’utero (della durata di 5-6 giorni). Durante questo cammino all’interno della tuba, la cellula uovo fecondata compie una serie di divisioni cellulari, che la porta a diventare una blastocisti. Quest’ultima s’impianta nella mucosa uterina e inizia a secernere un ormone, l’hCG (gonadotropina corionica umana) la cui presenza nelle urine o nel sangue della donna consente di scoprire lo stato di gravidanza.
Durante il primo trimestre di gravidanza, l’hCG stimola il corpo luteo a continuare a produrre estrogeni e progesterone, ormoni che consentono un corretto sviluppo dell’embrione. Il corpo luteo smette di funzionare dopo il terzo mese di gravidanza, quando cioè inizia l’attività della placenta, l’organo che consente gli scambi di sostanze nutrienti tra la madre e il feto e che sostituisce l’attività dell’ovaio per tutto il resto della gravidanza.
LE CAUSE DI INFERTILITÀ
La specie umana non è molto fertile. Si calcola che, per la donna, la possibilità di essere fecondata, se ha un rapporto nel periodo fertile, non superi il 25% e questa probabilità decresce con l’età dei partner. È classificata come “infertile” o “subfertile” la coppia che non ottiene un concepimento dopo 12 mesi di rapporti liberi e non protetti. E’ quindi evidente che una coppia debba concedersi un certo “periodo di prova” prima di definirsi infertile o subfertile. Secondo le linee guida dell’American Society for Reproductive Medicine, è giustificato iniziare accertamenti per determinare la presenza di uno o più ostacoli al concepimento solo dopo almeno 12 mesi di rapporti liberi e non protetti. Questo limite si abbassa a 6 mesi per le donne di età oltre 35 anni ed in presenza di fattori di rischio (pregressi interventi sugli organi pelvici, pregresse gravi infezioni utero ovariche, endometriosi etc.)
Esistono varie cause d’infertilità o sub-fertilità, che possono essere classificate in poche grandi categorie, che frequentemente possono coesistere tra loro. Una quota molto piccola di coppie viene definita sterile o affetta da sterilità assoluta (meno del 10%) quando sussistono condizioni che rendono impossibile l’ottenimento di una gravidanza.
Cause di Infertilità, subfertilità o sterilità assoluta
- Tubariche/pelviche: ostruzione o chiusura delle tube di Falloppio, aderenze pelviche
- Endometriosi: la presenza o la recidiva di una malattia spesso invalidante per la donna, ma talora asintomatica, che riduce in modo severo le probabilità di concepimento
- Ovulatorie/ormonali: mancanza o irregolarità dell’ovulazione, cicli irregolari, iperprolattinemia, sindrome dell’ovaio micropolicistico, ridotta o assente riserva ovarica
- Maschili: l’uomo non produce un numero sufficiente di spermatozoi, oppure essi non possiedono le caratteristiche di forma o di movimento adatti alla fecondazione, gli spermatozoi presentano anomalie strutturali oppure vengono prodotti anticorpi che agiscono contro gli spermatozoi
- Cervicali: il muco presente nella cervice uterina è ostile al passaggio degli spermatozoi per la presenza di fattori infettivi o per pregressi interventi chirurgici che hanno danneggiato le ghiandole cervicali
- Uterine: presenza di malformazioni congenite dell’utero, miomi o aderenze all’interno della cavità uterina oppure presenza di fattori infiammatori a carico dell’endometrio (la mucosa di rivestimento della cavità uterina)
- Sconosciute: Gli accertamenti non sono stati di grado di evidenziare una o più cause specifiche. Tale situazione va sotto il nome d’infertilità idiopatica o inspiegata. E’ spesso una diagnosi che dovrebbe essere correttamente definita come “insufficientemente indagata”, ma a cui si giunge per il lungo periodo di ricerca o l’età dei partner, che non consentono un completamento delle indagini.
COSA SI PUÒ FARE QUANDO SI HANNO PROBLEMI DI INFERTILITÀ
Con il termine PMA (procreazione medicalmente assistita) si definiscono le procedure mediche che supportano o vicariano uno o più aspetti della funzione procreativa al fine di consentire o di aumentare le probabilità di concepimento e d’impianto di una gravidanza.
La PMA cerca quindi di offrire una soluzione al problema dell’infertilità di coppia, quando il tempo di ricerca, gli accertamenti e la ricerca di alternative di cura hanno dato esito negativo o non sono percorribili.
Esistono due livelli di PMA:
- 1° livello: comprende le metodiche che hanno come obiettivo quello di aumentare la probabilità di concepire cercando di ottenere una fecondazione “in vivo”, ossia all’interno del corpo femminile. Ne fanno parte quindi:
- L’induzione dell’ovulazione per rapporti mirati
- L’inseminazione intrauterina (IUI o Intrauterine Insemination), metodica nella quale, dopo aver stimolato l’ovulazione con farmaci contenenti ormone follicolo-stimolante e aver monitorato ecograficamente e a volte con prelievi ormonali lo sviluppo dei follicoli, si deposita lo sperma del partner (opportunamente trattato e “capacitato”) direttamente in cavità uterina, al fine di favorire l’incontro con i gameti femminili (ovociti). E’ una procedura totalmente ambulatoriale
- 2°- 3° livello: si tratta della fecondazione in vitro. Con questa procedura, l’incontro tra ovocita e spermatozoo, e quindi la fecondazione, avviene al di fuori del corpo umano, in laboratorio. Richiede ricoveri in una struttura di Day Hospital per prelevare gli ovociti e per il successivo trasferimento in utero degli embrioni.
Dopo aver indotto un’ovulazione multipla attraverso la stimolazione delle ovaie, si procede al prelievo degli ovociti (pick-up ovocitario). Lo stesso giorno del prelievo degli ovociti il partner maschile procede alla raccolta del liquido seminale. Una volta ottenuti i gameti femminili e maschili, ci sono due possibilità di fecondazione:
- FIVET (fecondazione in vitro embryo transfer – IVF – In vitro Fertilization – è il termine con cui è nota nel mondo): con questa metodica ovociti e spermatozoi vengono posti insieme in una piastra con terreno di coltura adatto e si lascia che gli spermatozoi penetrino l’ovocita in modo naturale.
- ICSI (iniezione intracitoplasmatica dello spermatozoo): è la microiniezione di un singolo spermatozoo direttamente all’interno della cellula uovo. È riservata ai casi in cui si teme che, con la semplice inseminazione dell’ovocita, ci possano essere problemi nell’ottenere la fecondazione. È considerata metodica di PMA di III livello, quando sia necessario l’utilizzo di spermatozoi prelevati chirurgicamente dal testicolo.
Dopo la fecondazione, gli ovociti sono tenuti in coltura nel laboratorio di embriologia. Dopo 2-6 giorni dalla fecondazione sono trasferiti nell’utero della donna, mediante un intervento denominato embriotransfer.
- Il congelamento degli Ovociti: Congelamento e successivo scongelamento degli ovociti maturi non utilizzati al prelievo degli ovociti. Dopo scongelamento e ICSI gli embrioni vengono trasferiti in utero. E’ un’eccellenza Italiana, Paese in cui questa metodica è stata sviluppata e ha trovato i maggiori campi di applicazione. Inizialmente pensata per la preservazione della fertilità in pazienti oncologiche, ha trovato applicazione nelle coppie infertili che avessero ostacoli Etici al congelamento embrionario e per il lungo periodo (2004-2009) di divieto del congelamento embrionario e in questo momento per ridurre il numero di embrioni crioconservati. E’ la nuova frontiera per la preservazione di una possibile fertilità futura nelle donne che devono o scelgono di procrastinare la ricerca di una gravidanza.
- Il congelamento degli Embrioni: Il congelamento degli embrioni non trasferiti dopo il prelievo degli ovociti è la chiave per ridurre il numero delle gravidanze multiple, consentendo alla donna una possibilità di successo in caso di esito negativo del trattamento o di ottenere una nuova gravidanza anche in caso di esito positivo del ciclo di induzione.
Le procedure chirurgiche necessarie prevedono interventi minimamente invasivi e poco dolorosi e sono considerate a basso rischio chirurgico (le complicanze gravi sono, infatti, molto rare).
Le cose sono un po’ diverse se sono osservate dal punto di vista psicologico. Infatti, il trattamento prevede procedure che richiedono qualche cambiamento nel proprio stile di vita ed è’ inevitabile che chi si sottoponga a questo iter si senta esposto a un alto livello di stress emotivo e debba confrontarsi con nuove e impreviste insicurezze e preoccupazioni.
Fondamentalmente, l’ansia nasce tutta dalle stesse domande: andrà tutto bene? Riuscirò ad avere una gravidanza? Un bambino? Purtroppo è difficile stabilire a priori le probabilità che un trattamento vada a buon fine. La percentuale di successo dipende in modo importante dall’età della donna, ma altri fattori possono entrare in gioco e a volte è necessario ripetere lo stesso trattamento alcune volte prima di riuscire ad ottenere una gravidanza.
Il compito degli specialisti in Medicina della Riproduzione, che sono ostetrico ginecologi che hanno acquisito speciali competenze in ambito riproduttivo è non creare false aspettative, ma anche non spegnere giustificate speranze. Riteniamo che, laddove si sia fatta diagnosi d’infertilità, valga la pena di tentare la strada della procreazione medicalmente assistita, ma non è detto che tutte le coppie riescano così ad avere un bambino.
Il nostro compito come medici è di supportare e curare la donna e la coppia, anche perché curare non significa proporre nuovi tentativi o strategie inutili, ma aiutare a comprendere e a volte ad accettare che la medicina ‘onnipotente’ è una visione deviata della medicina moderna.
La possibilità di poter ricorrere, in condizione di grave e irreversibile impossibilità di concepire, ad una donazione di gameti maschili e/o femminili è in molte condizioni la sola possibilità di accesso ad una reale probabilità di gravidanza e di evoluzione favorevole della stessa. Questa possibilità è ora accessibile anche nel Nostro Paese, sebbene un Paese in cui la cultura della donazione è così poco sviluppata. La maggior parte dei gameti (ovociti e sperma) devono essere richiesti a Banche straniere.
LA PRESERVAZIONE DELLA FERTILITÀ MASCHILE
In caso di riscontro di patologia tumorale bisogna sempre informare i pazienti o i loro genitori che la Chemioterapia o la Radioterapia pelvica o gli interventi di chirurgia urologica per tumore testicolare o prostatico, di linfadenectomia o o di chirurgia addominale possono determinare infertilità. L’infertilità può essere in alcuni casi riconducibile a un danno irreversibile della produzione di spermatozoi, oppure alla scomparsa della eiaculazione. Questo danno dipende dallo schema terapeutico chemio-radioterapico, dalle dosi impiegate o dal tipo di chirurgia. La severità del danno non è però prevedibile di preciso. I bambini pre-puberi sono meno esposti a questo rischio ma anche in questo gruppo uno su tre avrà problemi a concepire in età adulta.Proporre la crioconservazione del liquido seminale prima dell’inizio delle terapie o degli interventi è considerato un atto obbligatorio per il Medico. In casi eccezionali, legati a neoplasie del sistema emopoietico che impongono un trattamento immediato al momento della diagnosi, pena il decesso del paziente, la crioconservazione non è praticabile anche per le condizioni precarie del paziente.
Non vi sono limiti di età per eseguire la procedura. Unica eccezione è il bambino prepubere.
Tecniche di Preservazione della Fertilità
- Crioconservazione del liquido seminale Si tratta di una procedura semplice e scevra di rischi che è entrata a far parte della normale pratica clinica. Il costo del servizio è per lo più standardizzato tra i Centri Lombardi e consiste in circa 200 euro per il congelamento e ulteriori 100 euro all’anno per il mantenimento. E’ eseguito di routine in tutti i Centri di II-III livello.
- TESE (Testicular Sperm Extraction) Quando il paziente non ha spermatozoi nel seme (5-10% dei casi), oppure quando non riesce ad eiaculare per motivi psicologici, oppure ancora quando il paziente è già stato sottoposto a chemioterapia e chirurgia senza aver prima crioconservato il seme, è possibile ricorre ad un piccolo intervento chirurgico (biopsia testicolare) che consente di estrarre e crioconservare spermatozoi. L’intervento si esegue in day hospital, anestesia locale o sedazione profonda e dura da 10 a 30 minuti.E’ una tecnica in espansione e dati preliminari riportano la possibilità di identificare spermatozoi in circa il 50% dei casi. Allo stato attuale l’Humanitas Fertility Center ha una delle maggiori casistiche internazionali in questo specifico campo della infertilità maschile
Informazioni per i pazienti
- I pazienti inviati per il congelamento del seme devono presentarsi con i seguenti esami (non più vecchi di 3 mesi): HBsAg, Anti HBc, Anti-HCV, Anti HIV-1 e 2, VDRL e TPHA.
- Non tutti i pazienti che risultano azoospermici al momento della raccolta resteranno tali.
- Alcuni riescono a recuperare la fertilità ed a procreare dopo pochi anni dalle terapie.
- Non vi sono tecniche di Fertility Preservation nel bambino prepubere. Sono in corso promettenti ricerche di base che puntano a isolare cellule staminali spermatogonali che potrebbero essere crioconservate e successivamente impiegate per ricolonizzare il testicolo. Non vi sono evidenze di efficacia nell’uomo e nessun Centro in Lombardia propone al momento la biopsia nel bambino con questa finalità.
- La TESE “in urgenza” (vale a dire entro una settimana) in pazienti oncologici che risultano azoospermici al momento della raccolta è disponibile presso l’Humanitas Fertility Center. Contattare il numero telefonico 02-8224 4646, oppure segreteria.medicinariproduzione@humanitas.it
VARICOCELE E INFERTILITÀ MASCHILE: MITI DA SFATARE
Non vale la pena operare il varicocele dopo i 30 anni.
E’ un dogma che resiste da molti decenni. Molte linee guida andrologiche ed urologiche sconsigliano la correzione chirurgica, asserendo una irreversibilità del danno provocato dal varicocele inveterato. Pertanto alle coppie con moglie giovane e marito dispermico quarantenne con varicocele viene di regola proposta la fecondazione medicalmente assistita.
Zini et al (2007) hanno studiato pazienti infertili con varicocele di età superiore a 40 anni. Una parte dei pazienti si è sottoposta a correzione chirurgica di varicocele mentre la restante si è rifiutata. I risultati in termini di gravidanza spontanea sono risultati clamorosamente favorevoli tra gli operati (49% vs. 21%), confermando così la reversibilità del danno gonadico da varicocele.
Anche nella nostra casistica i pazienti affetti da varicocele e di età compresa tra 36 e 48 anni hanno ottenuto gli stessi risultati in termini di miglioramento seminale (ovvero almeno il quadruplicamento del numero totale di spermatozoi con motilità progressiva) rispetto ai pazienti con meno di 36 anni (Negri L and Levi Setti PE, J Androl. 32:1, 2011).
Dopo la correzione chirurgica del varicocele lo spermiogramma peggiora per 6 mesi.
E’ una delle più suggestive leggende metropolitane che inducono le coppie a rinunciare all’intervento per non “perdere tempo” rispetto ad altre procedure riproduttive. Innanzitutto l’intervento chirurgico viene praticato in anestesia locale o in sedazione profonda (la stessa utilizzata per prelevare gli oociti per la ICSI), e queste anestesie non provocano alcun danno gonadico (nella donna e nell’uomo). Ma il dato più clamoroso è che la maggioranza delle gravidanze spontanee avviene entro i primi 6 mesi dopo l’intervento. Il 29% dei nostri pazienti la ottiene entro 3 mesi, un ulteriore 37% tra il terzo e il sesto mese ed un ulteriore 24% tra il sesto ed il dodicesimo mese.
Pertanto il miglioramento della capacità fecondante degli spermatozoi avviene in tempi rapidissimi. Questo non è necessariamente associato all’incremento del numero degli spermatozoi o della motilità. La moderna andrologia opera il varicocele per correggere l’eccesso di radicali liberi e quindi la perossidazione della membrana plasmatica degli spermatozoi, per ristabilire una normale reazione acrosomiale e per ridurre la frammentazione del DNA spermatozoario. E questi cambiamenti favorevoli avvengono in tempi molto più rapidi di quanto si possa pensare, con ripercussioni favorevoli anche sulle procedure di IVF/ICSI
(Larson et al., 2000; Larson-Cook et al., 2003; Saleh et al., 2003b; Tesarik et al., 2004; Werthman et al., 2007; Benchaib et al., 2007)
L’intervento è doloroso e la ripresa fisica è lunga
Da 15 anni effettuiamo interventi in day-hospital, utilizzando l’anestesia locale o la sedazione profonda (la stessa utilizzata per prelevare gli oociti per la ICSI). Ad oggi abbiamo eseguito 1.700 interventi e non abbiamo avuto una sola complicazione. Nessun paziente ci ha contattato nel post-operatorio per dolore o altri problemi. La tecnica mininvasiva subinguinale da noi utilizzata non contempla incisione di muscoli o fasce tendinee, quindi una attività lavorativa sedentaria può avviene entro 2-3 giorni vs. 5-7 giorni per lavori pesanti. L’attività sessuale e sportiva può essere ripresa dopo 7-10 giorni. La durata media dell’intervento è di 13 minuti; il paziente si alza per urinare e mangiare a distanza di 90 minuti dal termine dell’intervento e lascia l’Ospedale dopo 3 ore. Il tasso di recidiva/persistenza valutato con controllo ecocolordoppler risulta essere del 4% a 3 mesi dall’intervento.
AZOOSPERMA
L’azoospermia è l’assenza di spermatozoi nello sperma. Lo spermiogramma deve specificare che non ne sono stati osservati anche dopo centrifugazione del campione analizzato.
Quasi sempre la diagnosi è inaspettata perché il paziente non ricorda alcun problema genitale e questo crea un profondo turbamento.
L’azoospermia è un argomento di stretta attualità perché sembra sempre più frequente nella popolazione giovane.
La prime cose da fare sono:
- Ricontrollare l’esame seminale in un Centro di Infertilità perché a volte gli spermatozoi ricompaiono.
- Effettuare un prelievo del sangue ormonale (FSH, LH, testosterone totale, TSH)
- Effettuare un’ecografia testicolare con determinazione oggettiva del volume testicolare e descrizione accurata del tessuto testicolare
- Chiedere ai genitori se si è sofferto di problemi testicolari nell’infanzia, se si è nati prematuri o sottopeso, oppure se ci sono stati familiari con problemi di fertilità.
- Quindi rivolgersi a un Centro di Medicina della Riproduzione.
Questi esami, integrati alla vista e alla raccolta dettagliata della storia clinica, aiutano lo specialista in Medicina della Riproduzione (andrologo, urologo o endocrinologo) a orientarsi verso una diagnosi, perché le azoospermie non sono tutte uguali: alcune sono curabili, altre garantiscono elevate probabilità di avere un figlio con la ICSI, altre probabilità inferiori con la ICSI, infine altre che non hanno alcuna soluzione.
Schematicamente le azoospermia si suddividono in ostruttive o secretorie.
- Ostruttive (OA): la produzione di spermatozoi è sostanzialmente normale ma una ostruzione dei canali spermatici rende impossibile il loro transito nello sperma. Alcune possono essere legate a malformazioni delle vie seminali (come nelle mutazioni del gene della fibrosi cistica, oppure quando residui dell’apparato genitale femminile, che si trovano lungo i canali spermatici, non sono regrediti completamente ed ostacolano il passaggio dello sperma). Altre forme possono essere l’esito di infiammazioni/ infezioni/ traumi/ interventi chirurgici che hanno ostruito i canali spermatici. I casi tipici sono le infezioni a trasmissione sessuale contratte in gioventù, le prostatiti o le “cistiti”, gli interventi chirurgici per ernia inguinale (frequenti) o idrocele (frequenti). Fatti salvi casi molto rari, dove è possibile ricanalizzare le vie seminali e quindi ripristinare la fertilità spontanea (nella mia casistica sempre più rari negli italiani), il 99% di questi pazienti può realisticamente sognare di avere un figlio con la ICSI perché il 99% di loro ha spermatozoi nei testicoli. Gli spermatozoi possono essere recuperati con un piccolo intervento in anestesia locale (TESE), congelati ed utilizzati per più cicli di ICSI.
- Secretorie o non ostruttive (NOA): rappresentano l’altra faccia del problema, perché non ci sono ostruzioni ma esiste un problema nella “fabbrica” degli spermatozoi. Questo può essere
- genetico (anomalie cromosomiche occulte, delezioni del cromosoma Y, o più semplicemente un padre poco fertile)
- indotto da tossici ambientali (assenza di cellule staminali testicolari perché la madre è entrata in contatto, tra l’ottava e la tredicesima settimana di gestazione, con particolari sostanze chimiche ambientali e lavorative, alimentari, cosmetiche, ecc.)
- secondario ad eventi patologici come le torsioni dei testicoli, la tardiva discesa dei testicoli nella borsa scrotale (discesa spontanea o indotta con farmaci ormonali in epoca infantile, o con intervento chirurgico di orchipessi); oppure l’orchite parotitica (da “orecchioni”), le chemio-radioterapie per pregressi tumori (leucemie, linfomi, neoplasie osse), l’assunzione cronica di particolari farmaci (anti-rigetto per trapianti; farmaci per malattie autoimmuni). Una forma abbastanza rara ma “moderna” è quella delle sostanze dopanti.
Il 50 % di questi pazienti può realisticamente sognare di avere un figlio con la ICSI perché il 50% di loro ha spermatozoi nei testicoli e questi possono essere recuperati e crioconservati con la TESE. In questi casi, fatti salvi casi eccezionali, deve ricorrere alla procreazione medicalmente assistita (ICSI) con tassi di successo leggermente inferiori ai casi su base ostruttiva.
Sono azoospermico: potrò avere un figlio?
Tutto dipende un semplice esame del sangue e dall’età della partner: se il dosaggio del FSH è inferiore a 7.6 mu/ml e la partner non supera i 40 anni ci sono buone possibilità, perché le probabilità di trovare spermatozoi nei testicoli (TESE) e di avere un buon numero di ovociti dopo stimolazione ovarica sono ancora accettabili. Però bisogna rinunciare al sogno di avere un figlio in modo naturale. Quindi bisogna fare un “salto di qualità”, ed accettare di affidarsi a super-specialisti che cercheranno spermatozoi testicolari (TESE) da usare per una ICSI.
Nei pazienti che hanno una azoospermia ostruttiva (FSH inferiore a 7.6 mu/ml, testicoli di buon volume) e una moglie giovane, o con una buona riserva ovarica, le probabilità sono molto elevate. Se l’FSH maschile è alto e la partner è giovane abbiamo realisticamente il 50% delle probabilità di avere un figlio. L’unico caso dove non vale la pena di tentare è quando la riserva ovarica della partner sia esaurita e quando il paziente abbia particolari anomalie genetiche o del cromosoma Y.
Come si recuperano gli spermatozoi dai testicoli
Sono state finora descritte diverse tecniche di prelievo di spermatozoi. Alcune per recuperare spermatozoi dai testicoli (TEFNA, TESE, microTESE), altre dagli epididimi (PESA, MESA). A loro volta queste tecniche sono classificabili come vere e proprie procedure chirurgiche (TESE, microTESE e MESA) o come procedure di aspirazione con ago (TEFNA, PESA).
La nostra Scuola, dopo una esperienza maturata in 20 anni su migliaia di casi, è giunta alla conclusione che la TESE e, in casi molto selezionati, la microTESE rappresentano le tecniche chirurgiche con il migliore rapporto benefici/costi.
TESE (TEsticular Sperm Extraction)
Serve a recuperare spermatozoi da un piccolo frammento di tessuto testicolare asportato chirurgicamente. La TESE può essere effettuata in anestesia locale, loco-regionale o in sedazione profonda.
E’ utilizzabile in tutte le forme di azoospermia; è necessaria nelle NOA; consente il recupero e la crioconservazione del maggior numero possibile di spermatozoi. E’ ripetibile. Consente l’esecuzione di un esame istologico testicolare (per stabilire con chiarezza la causa della azoospermia ma principalmente per intercettare neoplasie testicolari occulte che nei pazienti NOA ammonta al 2.4%) (McLachlan et al., 2007). Trattandosi di una procedura chirurgica in regime di day-hospital è costosa, e il costo è giustificato dal trattamento del Laboratorio Embriologico che selezione e crioconserva gli spermatozoi. Per questo motivo poche strutture sanitarie nazionali ne garantiscono l’esecuzione con il Sistema Sanitario Nazionale. La struttura Ospedaliera dove operano i nostri specialisti garantisce tale procedura con il SSN. La crioconservazione delle provette di spermatozoi costa 200 euro all’anno. In Lombardia il trasporto degli spermatozoi in altri Centri costa 500 euro. Dopo l’intervento il paziente deve stare a riposo assoluto nelle 24-48 ore successive.
La nostra casistica
Nel periodo 2003-2011 il nostro gruppo ha eseguito 1142 TESE presso il Fertility Center di Humanitas. Si tratta di una delle maggiori casistiche internazionali ed i risultati sono in linea con i risultati dei migliori Centri Internazionali.
Il tasso di recupero di spermatozoi nei pazienti NOA risulta essere significativamente più elevato nel nostro Centro rispetto ai quelli estrapolati dalla recente review di Donoso et al., 2007) (Humanitas 381/654 vs 24 studi clinici da Pubmed 909/1838, p=0.0001). I risultati favorevoli non sono esclusivamente legati alla esperienza chirurgica ma anche alla qualità di Biologhe esperte nel trattamento e nella crioconservazione del prelievo testicolare.
LA FRAMMENTAZIONE DEL DNA SPERMATOZOARIO
L’integrità della cromatina spermatica è un requisito fondamentale per la fertilità maschile, ma non è rilevabile con lo spermiogramma. Una eccessiva frammentazione del DNA spermatico riduce le probabilità di concepimento naturale e con PMA di I livello. Livelli molto elevati di frammentazione del DNA spermatozoario possono compromette anche la PMA di II livello, riducendo i tassi di impianto dell’embrione e aumentando gli aborti precoci.
Siamo qui ogni volta che hai bisogno di noi
Telefono
02 5469 570 – 02 5466 596
Orari
Lunedì – Venerdì:
9:30/13:00
14:00/19:00
SO.GE.ME. s.r.l.
Via Podgora 11,
20122 – Milano
ISTITUTO MEDICO MILANESE
L’Istituto Medico Milanese è un centro polispecialistico di eccellenza, che offre le migliori competenze professionali a livello europeo, e dispone di apparecchiature all’avanguardia in un contesto di grande attenzione alle
esigenze del paziente.